Une plongée profonde dans la façon dont le nouveau coronavirus infecte les cellules a révélé qu’il orchestrait une prise de contrôle hostile de leurs gènes, contrairement à tout autre virus connu, produisant ce qu’un scientifique de premier plan appelle des changements « uniques » et « aberrantes ».
Les recherches les plus récentes lèvent le voile sur l’offensive du virus au cœur même de nos cellules. En détournant la lecture des segments d’ADN, le SARS-CoV-2 modifie les règles du jeu génétique. Ce phénomène éclaire pourquoi les seniors paient un tribut plus lourd au Covid-19, mais aussi pourquoi certains traitements antiviraux pourraient non seulement sauver des vies, mais potentiellement prévenir des formes graves s’ils sont administrés à temps.
« C’est une mécanique que je n’avais jamais observée en vingt ans de virologie », confie Benjamin TenoEver, chercheur à l’Icahn School of Medicine au Mount Sinai. Le SARS-CoV-2, responsable du Covid-19, s’approprie le génome cellulaire avec une habileté déconcertante.
L’équipe de TenoEver a constaté que ce coronavirus bloque toute une série de gènes de défense antivirale, tout en autorisant l’activation d’un autre groupe de gènes, une stratégie jamais vue chez les autres virus. À titre de comparaison, la grippe et le premier SARS (apparu au début des années 2000) perturbent simultanément les deux grandes branches de la réponse immunitaire : ce que TenoEver nomme les gènes « d’appel aux armes » et ceux « d’appel aux renforts ».
Pour mieux comprendre, voici comment fonctionnent ces deux groupes :
- Les gènes « d’appel aux armes » lancent la production d’interférons. Ces protéines, libérées par les cellules infectées, servent de signaux d’alerte : elles invitent les cellules alentour à activer près de 500 gènes destinés à ralentir la multiplication virale. Ce premier bouclier tient généralement entre sept et dix jours selon TenoEver, le temps de contenir l’invasion et de permettre à la seconde vague de défenses de se mobiliser.
- Le deuxième groupe, les gènes « d’appel aux renforts », produit des chimiokines. Ces molécules déclenchent une véritable mobilisation : les cellules B, productrices d’anticorps, et les lymphocytes T tueurs convergent vers la zone infectée. Si tout se déroule sans accroc, cette alliance retient le virus assez longtemps pour que les « professionnels » du système immunitaire passent à l’attaque.
Mais la plupart des virus classiques tentent d’entraver ces deux systèmes à différents degrés. Sans cette manœuvre, il serait quasiment impossible pour un virus de s’installer durablement dans l’organisme.
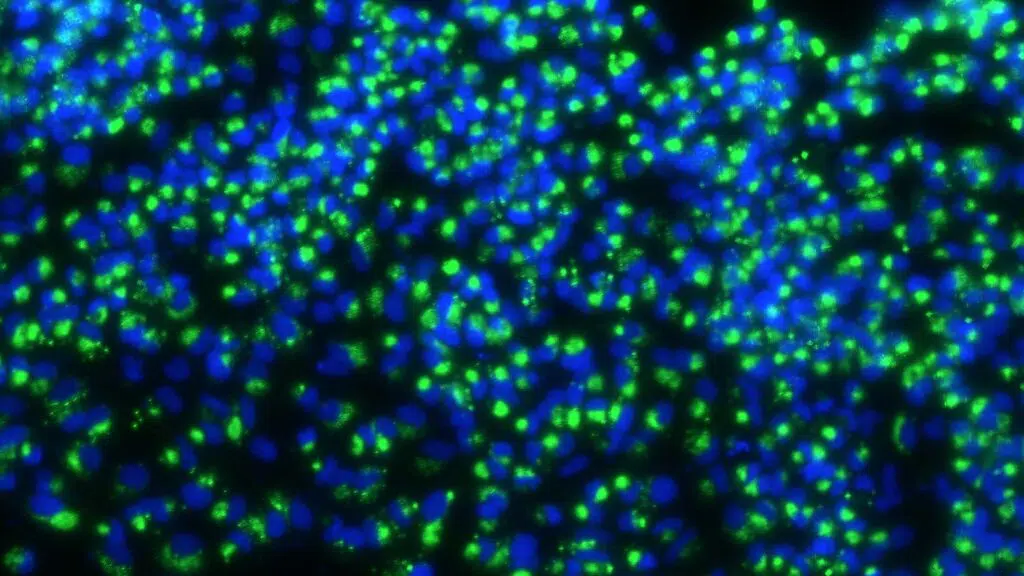
Le SARS-CoV-2, lui, joue une tout autre partition. Selon une publication parue dans Cell, l’équipe de TenoEver a analysé des cellules pulmonaires humaines cultivées en laboratoire, des furets (spécialement sensibles au virus) ainsi que des cellules pulmonaires issues de patients Covid-19. Résultat : dans chacun des cas, trois jours après infection, le virus force la production de cytokines par les gènes « d’appel aux renforts »… tout en muselant ceux chargés de produire les interférons, ces fameux freins à la réplication virale.
Résultat : la machine à dupliquer le virus tourne à plein régime, pendant qu’une tempête inflammatoire s’abat sur les poumons. Pour TenoEver, cette réaction « unique » et « aberrante » incarne la signature du SARS-CoV-2 sur le génome de ses victimes.
Au Japon, une équipe de chercheurs a récemment mis en lumière la stratégie moléculaire du virus. Le gène ORF3b du SARS-CoV-2 code une protéine, le facteur de transcription, dotée d’une « puissante activité anti-interféron », selon Kei Sato de l’Université de Tokyo. Cette arme est bien plus efficace que celle du premier SARS ou de la grippe : elle empêche la cellule de détecter la présence du virus et bloque l’expression des gènes de l’interféron.
Les analyses menées par l’équipe de l’Icahn School of Medicine n’ont d’ailleurs retrouvé aucune trace d’interféron dans les cellules pulmonaires de patients Covid-19. Privées de ces signaux, « rien n’entrave la prolifération du virus, qui envahit et détruit les poumons », explique TenoEver.
Face à cette absence de frein, les cellules pulmonaires intensifient l’appel aux renforts : elles libèrent toujours plus de signaux d’alerte, attirant macrophages, neutrophiles et autres cellules immunitaires. Cette surenchère de défense vire au cercle vicieux : une inflammation qui s’auto-alimente, jusqu’à saturer les tissus pulmonaires.
En parallèle, la multiplication incontrôlée du virus finit par tuer les cellules chargées d’assurer l’échange gazeux. Le scénario est brutal : difficulté respiratoire aiguë, hospitalisation en urgence.
Chez les plus âgés, mais aussi chez les personnes souffrant de diabète, de maladies cardiaques ou d’autres pathologies, la capacité d’activation des gènes « d’appel aux armes » est déjà réduite, avant même que le coronavirus ne fasse irruption. Le système immunitaire penche alors dangereusement vers une réponse inflammatoire excessive, sans parvenir à freiner la réplication virale.
Le constat que le SARS-CoV-2 inhibe fortement la production d’interférons a ouvert une piste inattendue : et si administrer ces molécules permettait d’éviter les formes graves, voire d’empêcher l’infection ? C’est ce que suggère Vineet Menachery, chercheur à l’Université du Texas.
Dans une étude menée sur des cellules humaines en laboratoire (publiée en préimpression, donc pas encore validée par les pairs), Menachery et son équipe ont observé que le SARS-CoV-2 empêche l’activation massive des gènes de l’interféron. Mais lorsque les cellules reçoivent de l’interféron IFN-1 avant d’être exposées au virus, celui-ci peine à se multiplier.
Quelques jours plus tard, la quantité de virus retrouvée dans les cellules traitées était 1 000 à 10 000 fois inférieure à celle mesurée dans des cellules non prétraitées. À noter : le virus du premier SARS, lui, résiste à l’interféron.
Jusqu’ici, le pari pour stopper la pandémie reposait sur un vaccin efficace et des antiviraux comme le remdesivir pour les formes sévères. Mais ces résultats génétiques mettent en lumière une troisième voie : les médicaments préventifs.
Selon Menachery, un traitement préventif à l’interféron de type 1 « pourrait stopper le virus avant qu’il ne s’établisse ».
Bien sûr, administrer un médicament à des personnes en bonne santé n’est jamais anodin. Les effets secondaires, notamment des symptômes grippaux, sont connus et ne sont tolérés qu’en cas de maladie avérée. Menachery le rappelle : « Le traitement à l’interféron n’est pas sans complications. » Les différentes formes d’interférons, déjà prescrites contre l’hépatite ou certains cancers, peuvent s’accompagner d’effets indésirables.
Mais l’équilibre entre les risques et les bénéfices pourrait évoluer, aussi bien à l’échelle individuelle que collective, si ces molécules ou d’autres médicaments réduisent la gravité du Covid-19, voire rendent l’infection quasi invisible.
Dans cette perspective, l’interféron agirait comme un signal d’alerte : il préparerait les cellules à l’arrivée du virus, ce qui pourrait limiter la propagation et renforcer la résistance. Reste à confirmer tout cela, bien sûr, par des essais cliniques, déjà en cours.
Le combat contre le SARS-CoV-2 se joue ainsi dans l’arène microscopique du génome ; un bras de fer entre les mécanismes de défense ancestraux et l’ingéniosité virale. Les prochaines semaines diront si la science parvient à inverser ce rapport de force.